2023年9月,長聖國際生技CAR.BiTE-γδT取得美國FDA IND核准,其最大特色是在於可解決現今CAR-T療法無法有效治療實體癌 (solid tumor) 之瓶頸,也創下異體細胞治療 (Allogeneic Cell Therapy) 的新里程碑。為跟上全球癌症治療的趨勢以及台灣通過在即的再生醫療法,為此,禮文引進多年經驗的檢體供應商-AllCells,提供GMP-compliant人類白血球單採細胞 (Leukopaks),以協助推動異體細胞產品從研發到製程,滿足與日俱增的市場需求。
*AllCells在美國CGT產業已耕耘超過30年,擁有FDA登記血液中心、CLIA認證實驗室、血液庫及組織庫的許可證,已供應細胞材料給國內外多家藥廠及CDMO/CRO公司,進行異體細胞治療的研發、製程開發及商品化,產品品質值得信賴。*
異體細胞製劑的成功關鍵在於細胞材料的品質!
細胞從產出到取得過程中的每一步驟皆至關重要,AllCells在收集前透過問卷及血液檢測等方式評估捐贈者的合適性 (Donor eligibility),且在符合IRB的規範下,於封閉式的系統中以白血球分離術 (Leukapheresis) 收集檢體,將污染的機會降至最低,且以最佳化的冷凍程序保存細胞,並為捐贈者建立可追溯的資料庫,而禮文也堅持採用冷鏈運輸 (dry ice/liquid nitrogen) 將產品配送到府,維持細胞的高品質及高存活率 (> 90%)。
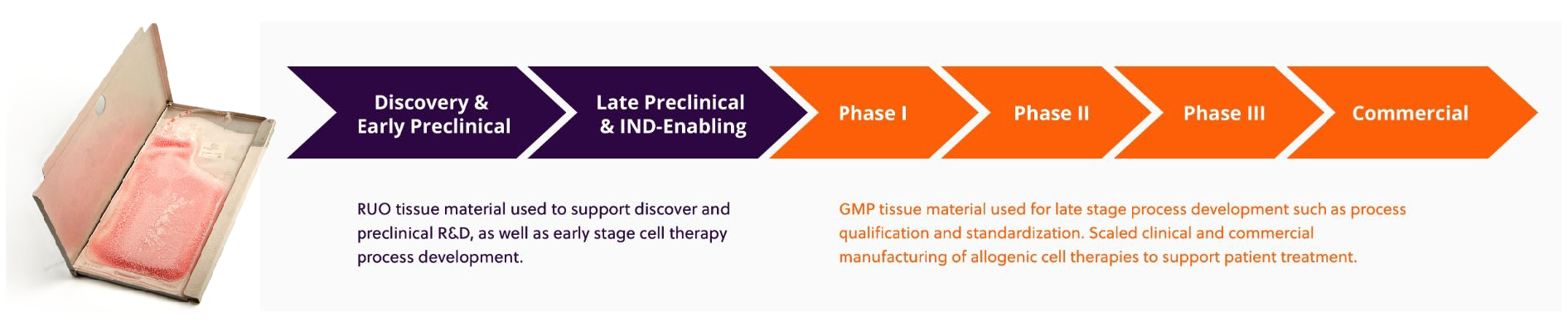
AllCells RUO和GMP-compliant細胞材料究竟有什麼不同?
為了堅守細胞品質的一致性,兩者在細胞的取得、保存與運送皆如上所述,讓您在不同開發階段的銜接上無痛轉換細胞材料,而最大差異則在於GMP-compliant產品符合AABB及FDA 21 CFR 1271之規範,經多達10項病原檢測陰性,可作為大量起始材料供製程開發、臨床試驗及取得藥證後的製程所需,而RUO產品僅供研究使用,具備HIV/HBV/HCV陰性,可作為早期研發及臨床前的實驗材料。因此,您可依使用需求選擇RUO或GMP-compliant產品,免去自行收案所要耗費的繁瑣流程,快速取得價格實惠且品質優良的細胞。
尚未擴大實驗規模?
AllCells尚提供初代細胞冷凍小管,包括PBMC、CD34 HSPC、純化免疫細胞 (B cell/T cell/NK cell/Monocyte) 等,更多資訊請參考:
異體細胞治療(上) 從基礎研究到製程開發-RUO細胞材料
想要自行開案收集?
禮文代理的QualTex Laboratories可為您提供細胞治療檢測服務,包括捐贈者合適性評估 (Donor Screening)、初始材料及最終產品的檢測 (Product Testing) 等,更多資訊請參考:
針對上述資訊若有興趣,歡迎進一步與我們洽詢。
