近年來,嵌合抗原受體T細胞療法(CAR-T)已成為腫瘤免疫治療的重要策略之一。然而,傳統Ex vivo CAR-T需先從患者體內分離出T細胞,於體外進行基因編輯與細胞擴增後輸回患者體內。此做法不僅製造流程複雜、成本高昂且耗時數週,最終成品需仰賴冷凍保存與冷鏈運輸,該過程可能影響細胞品質與治療穩定性。此外,Ex vivo CAR-T通常透過病毒載體導入CAR DNA,可能伴隨永久性基因整合錯誤的潛在風險。隨著全球生技製藥產業的迅速發展,體內生成CAR-T(In vivo CAR-T)技術逐漸受到關注,透過不同基因遞送技術,將CAR基因(RNA或DNA)直接導入患者體內T細胞,使其表達目標蛋白並達到治療效果,進一步實現off-the-shelf現成療法。
常見的基因遞送技術包括非病毒奈米載體系統(脂質奈米顆粒(LNP)與外泌體(Exosome))以及病毒載體系統,可攜帶目標基因之mRNA、circular RNA(cRNA)或DNA。隨著基因遞送技術持續發展並於初步臨床研究中取得成功,數家國際藥廠紛紛投入並加速布局In vivo CAR-T市場,例如Eli Lilly取得具cRNA LNP技術的Orna、AbbVie取得開發targeted LNP(tLNP)-mRNA In vivo CAR-T平台的Capstan Therapeutics,而Kite/Gilead則取得具targeted lentiviral DNA delivery技術的Interius BioTherapeutics1,2,3。台灣亦有知名製藥業者開發標靶外泌體遞送平台,並推進至臨床試驗階段,反映新世代細胞與基因治療技術的發展趨勢,並突顯In vivo CAR-T在未來臨床應用上的潛力。
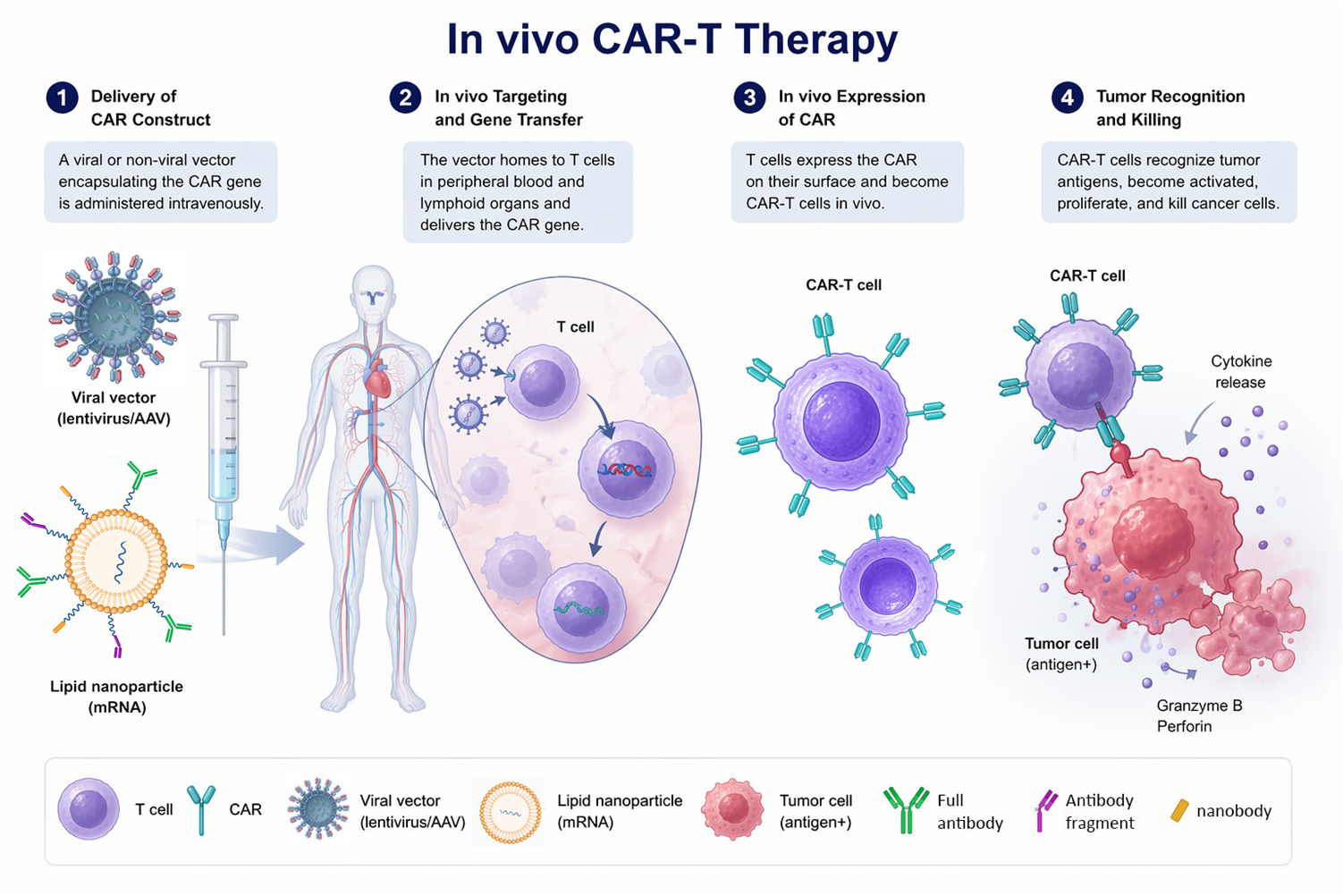
除了基因遞送技術外,如何將載體精準導向目標T細胞亦是治療成敗的關鍵因素。基因遞送載體可搭配不同的標靶,以提升遞送效率。常見的標靶包括特異性抗體/抗體片段(如scFv/VHH)、配體(Ligand)以及病毒包膜蛋白(Viral envelope protein),可促進載體與特定T細胞表面受體的專一性結合。其中,scFv/VHH等抗體片段因具高度專一性,已成為In vivo CAR-T設計中的關鍵要素。以LNP載體為例,可透過表面修飾scFv/VHH,將CAR mRNA精準遞送至目標T細胞,使其於體內短暫表達CAR,進而賦予其辨識特定抗原的能力,並誘導後續細胞毒殺反應。隨著基因遞送技術與標靶設計的演進,In vivo CAR-T顯示體內細胞改造的可行性,並展現其在臨床應用上的潛力。
1. 禮來斥資 24 億美元收購 Orna Therapeutics,進軍體內 CAR-T 療法 | GeneOnline News
